已知溶液中存在平衡:Ca(OH)2(s) Ca2+(aq)+2OH-(aq) △H
Ca2+(aq)+2OH-(aq) △H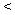 0,要想使c(Ca2+)减少,c(OH-)增多,可以采取的措施( )
0,要想使c(Ca2+)减少,c(OH-)增多,可以采取的措施( )
①升高温度,②向溶液中加入少量碳酸钠粉末,③加入少量MgCl2固体,
④加入少量KCl固体,⑤加入少量Ba(OH)2固体,⑥恒温下,加入氧化钙
- A.①④⑥
- B.②③⑤
- C.③⑤
- D.②⑤
答案
正确答案:D
知识点:影响沉淀溶解平衡的因素
①升高温度,平衡向吸热方向移动即逆向移动,c(Ca2+)和c(OH-)都减小,故①错误;
②向溶液中加入少量碳酸钠粉末,c(Ca2+)减小,平衡正向移动,c(OH-)增大,故②正确;
③向溶液中加入少量MgCl2固体,c(OH-)减小,平衡正向移动,c(Ca2+)增大,故③错误;
④向溶液中少量KCl固体,不影响平衡的移动,c(Ca2+)和c(OH-)不变,故④错误;
⑤向溶液中加入少量Ba(OH)2固体,c(OH-)增大,平衡逆向移动,c(Ca2+)减小,故⑤正确;
⑥恒温下,加入氧化钙,发生CaO+H2O![]() Ca(OH)2,仍为饱和溶液,c(Ca2+)和c(OH-)不变,故⑥错误;
Ca(OH)2,仍为饱和溶液,c(Ca2+)和c(OH-)不变,故⑥错误;
综上分析,要想使c(Ca2+)减少,c(OH-)增多,可以采取的措施有②⑤,所以选项D正确。
故选D。
略







