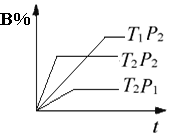
已知某可逆反应mA(g)+nB(g) qC(g)在密闭容器中进行,下图表示此反应在不同时间下,温度T和压强p与反应物B在混合气体中的百分含量B%的关系曲线。下列判断正确的是( )
qC(g)在密闭容器中进行,下图表示此反应在不同时间下,温度T和压强p与反应物B在混合气体中的百分含量B%的关系曲线。下列判断正确的是( )
- A.T1<T2,p1<p2,m+n<q,正反应吸热
- B.T1>T2,p1>p2,m+n>q,正反应吸热
- C.T1>T2,p1>p2,m+n<q,正反应放热
- D.T1<T2,p1<p2,m+n>q,正反应放热
答案
正确答案:A
知识点:温度对化学平衡的影响 百分含量与时间的图象 压强对化学平衡的影响
“定一议二”原则:图象中有三个量时,先确定一个量不变,再讨论另外两个量的关系。
“先拐先平,数值大”原则:在化学平衡图象中,先出现拐点的反应先达到平衡状态,先出现拐点的曲线所代表的反应温度较高或压强较大。
当温度为T2时,根据“先拐先平,数值大”原则可知,p2>p1,且压强越大,B%越大,说明增大压强平衡逆向移动,即逆反应气态物质系数减小,m+n<q。当压强为p2时,根据“先拐先平,数值大”原则可知,T2>T1,且温度越高,B%越小,说明升高温度平衡正向移动,即正反应为吸热反应。综上,A正确。
故选A。
略








